Sind wir alle vor Diabetes?
 Selbst wenn ein Arzt Ihnen versichert, dass Ihr Blutzucker "normal" ist, zeige alarmierende Beweise, dass Sie einem erheblichen Risiko eines vorzeitigen Todes ausgesetzt sind, es sei denn, Sie erreichen eine optimale 24-Stunden-Glukosekontrolle.m
Selbst wenn ein Arzt Ihnen versichert, dass Ihr Blutzucker "normal" ist, zeige alarmierende Beweise, dass Sie einem erheblichen Risiko eines vorzeitigen Todes ausgesetzt sind, es sei denn, Sie erreichen eine optimale 24-Stunden-Glukosekontrolle.m
Life Extension® warnte schon vor den stillen Gefahren, wenn der Blutzucker nüchtern über 85 mg / dl liegt. Neue wissenschaftliche Studien belegen diese Position.
Noch heimtückischer sind Daten, die zeigen, dass Blutzuckerspitzen die nach jeder Mahlzeit auftreten, das Risiko für Herz-Kreislauf-Erkrankungen, Netzhautschäden und Krebs erhöhen.
Wenn nicht Schritte unternommen werden, um die Zuckerstöße nach dem Essen zu unterdrücken, kann jede große Mahlzeit, die Sie essen, eine gefährliche Stoffwechselkaskade auslösen, die zu Zellschäden und beschleunigtem Altern führt.
Glücklicherweise gibt es bewährte Methoden, um den Blutzucker den ganzen Tag über optimal zu unterstützen.
Der neueste ist ein Extrakt aus grünen Kaffeebohnen, der auf ein kritisches Enzym abzielt, das an Blutzuckerspitzen nach der Mahlzeit beteiligt ist. In einer placebokontrollierten Menschenstudie führte dieser natürliche Extrakt zu erstaunlichen um 32% niedrigeren Blutzucker nach einer Mahlzeit! 1
Eine Epidemie von erhöhtem Blutzucker
 Der Prozentsatz der Erwachsenen, die unter chronisch hohem Blutzucker leiden, ist erstaunlich!
Der Prozentsatz der Erwachsenen, die unter chronisch hohem Blutzucker leiden, ist erstaunlich!
In einem Bericht wurden 46.000 Personen im mittleren Alter bewertet und es wurde festgestellt, dass über 80% Nüchternblutzucker von 85 mg / dl oder mehr hatten.2
Eine andere Studie mit 11.000 Personen mittleren Alters und älteren Menschen zeigte, dass 85% Nüchternblutzucker von 85 mg / dl oder mehr hatten.3
Da die Inzidenz von Krankheiten zuzunehmen beginnt, wenn der Blutzucker nüchtern über diese Werte steigt, bedeutet dies, dass die große Mehrheit der alternden Menschen heute chronische Zellschäden erleidet, die mit erhöhtem Blutzucker verbunden sind.
Diese Epidemie mit erhöhtem Blutzucker beschleunigt die altersbedingte Erkrankung, bis der Arzt erkennt, dass ihre Testwerte für die Bestimmung des "normalen" Blutzuckers schrecklich fehlerhaft sind.
Schwerwiegende Mängel des Mainstream-Medikaments
 Es gibt zwei Hauptprobleme bei der Art und Weise, wie die allgemeine Medizin den Blutzucker betrachtet.
Es gibt zwei Hauptprobleme bei der Art und Weise, wie die allgemeine Medizin den Blutzucker betrachtet.
Erstens ist der "normale" Bereich für Nüchternblutzucker immer noch zu hoch eingestellt. Die aktuellen Kriterien legen fest, dass Sie nicht "Diabetiker" sind, es sei denn, der Blutzuckerwert bei Fasten übersteigt 125 mg / dl. Der Bereich zwischen 100 und 125 mg / dl wird als "Prä-Diabetiker" betrachtet. 4 Mit einem Blutzuckerwert von 99 mg / dL wird Ihr Arzt Ihnen sagen, dass alles in Ordnung ist, und Sie unkenntlich von den lauernden Gefahren nach Hause schicken.
Erinnern Sie sich daran, dass eine optimale Glukosekontrolle stattfindet, wenn Fasten Blutzucker zwischen 70 und 85 mg / dl gehalten wird. Dies bedeutet, dass der Blutzuckerspiegel, der heute von Ärzten als "normal" eingestuft wird, in Wirklichkeit gefährlich erhöht ist.
Zweitens informieren Mainstream-Ärzte ihre Patienten nicht über die Risiken von Blutzuckerspitzen nach der Mahlzeit (Postprandial). Diese plötzlichen Blutzuckerschäden schädigen nach jeder Mahlzeit empfindliche Blutgefäße in Gehirn, Herz, Nieren und Augen und beschleunigen das Altern der Zellen und Gewebe im gesamten Körper.
Wenn Sie nur die Blutzuckermessungen des Fastens verwenden, werden keine gefährlichen Glukosespitzen nach einer Mahlzeit festgestellt, die ein erhöhtes Todesrisiko darstellen.5.6 Die entscheidende Wahrheit ist, dass Standarddefinitionen von Diabetes gefährlich veraltet sind.
 Wissenschaftliche Forschungen zeigen, dass die nach der Mahlzeit auftretenden Spitzen im Blutzucker möglicherweise schädlicher als Erhöhungen des Nüchternblutzuckers sind.7-10 Zum Beispiel bei Menschen mit "normalen" Blutzucker und "normalen" Blutzuckertoleranztests erhöht sich das Risiko eines Herzinfarkts um 58% für jeden Anstieg der Blutzuckerwerte nach der Mahlzeit um 21 mg / dl11. Bei einer ähnlichen Erhöhung der Glukose nach dem Essen, steigt das Risiko von Herz-Kreislauf-Erkrankungen zu sterben um 26% .12 Die Kontrolle der Glukose nach einer Mahlzeit muss als kritische Komponente bei der Verringerung kardiovaskulärer Komplikationen anerkannt werden.13
Wissenschaftliche Forschungen zeigen, dass die nach der Mahlzeit auftretenden Spitzen im Blutzucker möglicherweise schädlicher als Erhöhungen des Nüchternblutzuckers sind.7-10 Zum Beispiel bei Menschen mit "normalen" Blutzucker und "normalen" Blutzuckertoleranztests erhöht sich das Risiko eines Herzinfarkts um 58% für jeden Anstieg der Blutzuckerwerte nach der Mahlzeit um 21 mg / dl11. Bei einer ähnlichen Erhöhung der Glukose nach dem Essen, steigt das Risiko von Herz-Kreislauf-Erkrankungen zu sterben um 26% .12 Die Kontrolle der Glukose nach einer Mahlzeit muss als kritische Komponente bei der Verringerung kardiovaskulärer Komplikationen anerkannt werden.13
Ärzte wissen nicht, dass ein isolierter Nüchternglukose Wert während des ganzen Tages keine Informationen über die Blutzuckerkontrolle ihrer Patienten liefert. Wenn ein Patient beispielsweise einen Nüchternglukose-Wert von beispielsweise 95 mg / dl hat, kann dies eine künstlich niedrige Zahl sein, die nicht den realen Zustand des Patienten widerspiegelt.
Beispielsweise verbringt ein Patient mit einem Nüchternglukose von 95 mg / dL den größten Teil des Tages deutlich über 150 mg / dL, da sein alternder Körper nicht in der Lage ist, die Auswirkungen der übermäßig aufgenommenen Kalorien zu neutralisieren.
Ohne Kontrolle des Fastens und der postprandialen Zuckerspitzen ist das Stadium einer beschleunigten Alterung und einer Reihe von degenerativen Erkrankungen eingestellt.
Warum wir zu erhöhter Glukose neigen
 Wenn der Blutzucker jemals zu niedrig fällt, kommt es schnell zum Tod, da die Gehirnzellen ohne ausreichende Glukose nicht lange funktionieren können. Um sich vor dem akuten Tod in dem Zustand zu schützen, in dem unsere Vorfahren fast verhungern, hat der Körper Ausgleichsmechanismen entwickelt, um sicherzustellen, dass der Blutzuckerspiegel nicht zu tief sinkt.
Wenn der Blutzucker jemals zu niedrig fällt, kommt es schnell zum Tod, da die Gehirnzellen ohne ausreichende Glukose nicht lange funktionieren können. Um sich vor dem akuten Tod in dem Zustand zu schützen, in dem unsere Vorfahren fast verhungern, hat der Körper Ausgleichsmechanismen entwickelt, um sicherzustellen, dass der Blutzuckerspiegel nicht zu tief sinkt.
Das Problem bei diesen Schutzmechanismen besteht darin, dass die Mehrheit der heute alternden Menschen einen gefährlich erhöhten Blutzucker erleidet, da in modernen Gesellschaften keine weit verbreitete Hungersnot mehr besteht.
Wie tritt chronische Glukose-Überladung auf?
 Während die Glykogenolyse unsere Vorfahren vor akutem Hunger und Tod bewahrt hat, sind die Auswirkungen auf die Menschen heute das Gegenteil. Wenn wir älter werden, führt dieser interne Kontrollmechanismus (Glykogenolyse) zu Fehlfunktionen, was gefährlich hohe Blutzuckerspiegel zur Folge hat.
Während die Glykogenolyse unsere Vorfahren vor akutem Hunger und Tod bewahrt hat, sind die Auswirkungen auf die Menschen heute das Gegenteil. Wenn wir älter werden, führt dieser interne Kontrollmechanismus (Glykogenolyse) zu Fehlfunktionen, was gefährlich hohe Blutzuckerspiegel zur Folge hat.
Ein weiterer Faktor, der erhöhte Glukose verursacht, ist die übermäßige Schaffung von neuer Glukose im Körper. Bei gesunden Menschen erzeugt ein biochemischer Prozess, der als Gluconeogenese bezeichnet wird, neue Glukose aus anderen Substanzen wie Aminosäuren, wenn der Blutzuckerspiegel zu niedrig ist. Menschen, die älter werden, machen aus allen Lebensmitteln zu viel Glukose, selbst wenn der Blutzuckerspiegel bereits zu hoch ist.
Entgegen der landläufigen Meinung sind Kohlenhydrate nicht die einzige Nahrungsquelle für Blutzucker. Aminosäuren, die in Proteinen gefunden werden, wandeln sich durch Gluconeogenese leicht in Blutzucker um.
Ein Enzym, das an der Glukoneogenese und der Glykogenolyse beteiligt ist, ist Glukose-6-Phosphatase.
Mit zunehmendem Alter und steigenden Blutzuckerspiegeln, kann die Kontrolle der Glukose-6-Phosphatase beeinträchtigt werden. Wenn dies der Fall ist, erhöht Glukose-6-Phosphatase die Freisetzung von gespeicherter Glucose aus der Leber (Glykogenolyse) und erhöht die Glucosebildung (Gluconeogenese)… trotz bereits ausreichender Blutzuckerspiegel nach der Mahlzeit.
Aufgrund der übermäßigen Aktivität von Glukose-6-Phosphatase ist es für viele ältere Menschen nahezu unmöglich, optimale Glukosespiegel zu erreichen. Verbindungen, die auf Glukose-6-Phosphatase abzielen, werden aggressiv gesucht, um einer Diabetes-Epidemie entgegenzuwirken, die sich in den letzten drei Jahrzehnten in den Vereinigten Staaten nahezu verdreifacht hat.
 Da konventionelle medizinische Behörden Patienten immer noch nicht als "Diabetiker" diagnostizieren, bis sie über 125 mg / dl Nüchternglukose oder über 199 mg / dl Glukose nach der Mahlzeit zeigen, bleibt die tatsächliche Zahl der Menschen, deren Gesundheit durch hohen Blutzucker zerstört wird, nach wie vor bestehen grob unterschätzt.
Da konventionelle medizinische Behörden Patienten immer noch nicht als "Diabetiker" diagnostizieren, bis sie über 125 mg / dl Nüchternglukose oder über 199 mg / dl Glukose nach der Mahlzeit zeigen, bleibt die tatsächliche Zahl der Menschen, deren Gesundheit durch hohen Blutzucker zerstört wird, nach wie vor bestehen grob unterschätzt.
Daten zeigen beispielsweise, dass das Risiko für einen Schlaganfall steigt, wenn die Glukose im Nüchternzustand 83 mg / dl überschreitet. Jede Erhöhung um 18 mg / dL über 83 hinaus führt zu einem um 27% höheren Risiko, an einem Schlaganfall zu sterben.14 Wenn es also nicht gelingt, die Glukosewerte aggressiv zu senken, setzt dies die große Mehrheit der amerikanischen Bevölkerung der Hauptursache für Langzeitbehinderungen aus dritthöchste Todesursache, dh Schlaganfall.
Selbst die Einhaltung einer kalorienreduzierten Diät oder einer Diät mit niedrigem Kohlenhydratgehalt schützt nicht immer vor den durch Glukose-6-Phosphatase ausgelösten Glukosespiegeln.
Zusammenfassend lassen sich zwei interne Faktoren zusammenfassen, die zur Erhöhung des Blutzuckerspiegels beitragen:
- Glykogenolyse - Freisetzung von gespeicherter Glukose aus der Leber.
- Glukoneogenese - Erzeugung von neuer Glukose aus Nichtkohlenhydraten.
Die übermäßige Expression von Glukose-6-Phosphatase ist an der Glykogenolyse und Gluconeogenese beteiligt. Die Unterdrückung der Glukose-6-Phosphatase bietet eine entscheidende Strategie zur Begrenzung der zerstörerischen Auswirkungen eines erhöhten Blutzuckers nach der Mahlzeit.
Bekämpfung von Glukose im Überschuss mit Chlorogensäure
 Auf der Suche nach natürlichen Wegen, um Blutzuckerspitzen nach einer Mahlzeit sicher zu hemmen, richteten die Wissenschaftler ihre Aufmerksamkeit auf Pflanzenstoffe, die auf das Glukose-6-Phosphatase-Enzym abzielen.
Auf der Suche nach natürlichen Wegen, um Blutzuckerspitzen nach einer Mahlzeit sicher zu hemmen, richteten die Wissenschaftler ihre Aufmerksamkeit auf Pflanzenstoffe, die auf das Glukose-6-Phosphatase-Enzym abzielen.
Pharmazeutische Forscher strebten nach einem Medikament, das sich nach der Mahlzeit auf Blutzuckerspitzen stützen könnte.15,16 Idealerweise würde dieses Medikament die Glucose-6-Phosphatase unterdrücken, die an der Bildung von neuem Glukose und der Freisetzung von Glukose aus seiner Lagerungsstelle in beteiligt ist die Leber. 15-18
Aufregende neue Erkenntnisse zeigen, dass eine natürliche Verbindung innerhalb der grünen Kaffeebohne, die als Chlorogensäure bekannt ist, Blutzuckerspitzen nach der Mahlzeit modulieren kann.
Wie aus einer Vielzahl von Studien hervorgeht, ist der Kaffeekonsum mit einem geringeren Risiko für Typ-2-Diabetes verbunden.19-23 Wir verstehen nun, dass Chlorogensäure in Kaffee erhebliche antidiabetische Eigenschaften ausübt. Und wie jüngste Studien zeigen, besteht bei 80 bis 85% der erwachsenen Bevölkerung ein Risiko für diabetische Komplikationen, da der Blutzuckerspiegel zu hoch ist! 2
Grüner Kaffee-Extrakt verbessert die Glukosekontrolle
 Grünkaffee-Bohnen-Extrakt, der in nicht gerösteten Kaffeebohnen gefunden wird, produziert, sobald er gereinigt und standardisiert ist, hohe Mengen an Chlorogensäure und anderen nützlichen Polyphenolen, die übermäßige Blutzuckerwerte unterdrücken können.
Grünkaffee-Bohnen-Extrakt, der in nicht gerösteten Kaffeebohnen gefunden wird, produziert, sobald er gereinigt und standardisiert ist, hohe Mengen an Chlorogensäure und anderen nützlichen Polyphenolen, die übermäßige Blutzuckerwerte unterdrücken können.
Klinische Studien am Menschen unterstützen die Rolle von Chlorogensäure-reichen grünen Kaffeebohnen-Extrakten bei der Förderung einer gesunden Blutzuckerkontrolle und der Verringerung des Krankheitsrisikos.
Im Wissen um die entscheidende Bedeutung der Kontrolle von Blutzuckerspitzen nach der Mahlzeit, haben Wissenschaftler eine Studie unter 56 gesunden Personen durchgeführt
Freiwillige, die sie mit einem oralen Glukosetoleranztest vor und nach einer Ergänzungsdosis Rohkaffee-Extrakt fordern. Der orale Glukosetoleranztest ist eine standardisierte Methode zur Messung der Blutzuckerreaktion einer Person nach einer Mahlzeit.
Bei Probanden, die kein Extrakt aus grünen Kaffeebohnen einnahmen, zeigte der orale Glukosetoleranztest den erwarteten Anstieg des Blutzuckers nach 30 Minuten auf einen Durchschnittswert von 144 mg/dL. Aber bei Probanden, die 200 mg Extrakt aus grünen Kaffeebohnen genommen hatten, war diese Zuckerspitze deutlich reduziert, auf 124 mg / dl - ein Rückgang von 14%1 (Siehe Abbildung 1).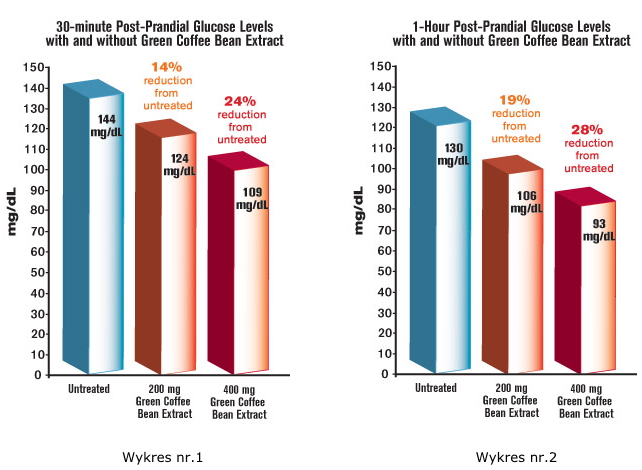
Dieser beeindruckende Unterschied hielt während der zweistündigen Studienperiode bei einer so niedrigen Dosis an 200 mg von Extrakt aus grünen Kaffeebohnen. Die Probanden hatten eine durchschnittliche Blutzuckersenkung um 19% nach einer Stunde und eine 22% Reduktion (Glukose auf nur 89 mg / dL ) nach zwei Stunden, verglichen mit den unbehandelten Werten jedes Patienten. Mit anderen Worten, die Anzahl der Personen, die Glukosewerte im gefährlichen Bereich hatten, wurde durch den Extrakt von grünen Kaffeebohnen stark eingeschränkt1 (Siehe Abbildungen 1 und 2).
Anders ausgedrückt, wenn die Probanden den Extrakt aus grünen Kaffeebohnen nicht genommen haben, zeigte Ihr oraler 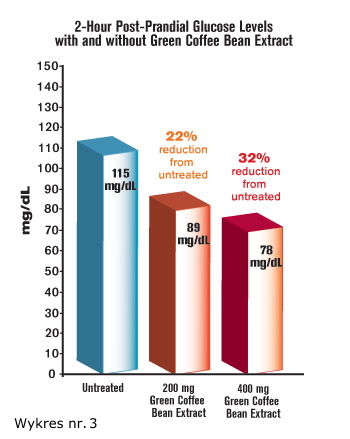 Glukosetoleranzwert nach zwei Stunden einen Blutzuckerwert von 115 mg / dl - ein höher als wünschenswerter Wert. Bei einer bescheidenen Dosis von 200 mg Extrakt aus grünen Kaffeebohnen sanken die Blutzuckerwerte von zwei Stunden nur auf 89 mg/dL1 (Siehe Abbildung 3).
Glukosetoleranzwert nach zwei Stunden einen Blutzuckerwert von 115 mg / dl - ein höher als wünschenswerter Wert. Bei einer bescheidenen Dosis von 200 mg Extrakt aus grünen Kaffeebohnen sanken die Blutzuckerwerte von zwei Stunden nur auf 89 mg/dL1 (Siehe Abbildung 3).
Für die meisten alternden Personen ist es auch schwierig acht bis zwölf Stunden nach dem Essen einen Glukosewert im Fasten von 89 mg / dl zu erreichen. Als diese Versuchspersonen jedoch 200 mg Extrakt aus grünen Kaffeebohnen nahmen, fielen Ihre Glukosespiegel nur zwei Stunden nach dem Trinken einer reinen Glukoselösung auf 89 mg / dL. Das hochdosierte Glukosegetränk wird standardmäßig verwendet. Orale Glukosetoleranztests erhöhen den Blutzucker stärker als typische Mahlzeiten.
Wenn eine höhere Dosis ( 400 mg ) vom Extrakt aus grünen Kaffeebohnen vor einer Dosierung verabreicht wurde, gab es eine größere durchschnittliche Reduktion des Blutzuckers - bis zu 28% nach einer Stunde!1
Wie der Extrakt aus grünen Kaffeebohnen die Glukoseerhöhung unterdrückt
Wissenschaftler haben entdeckt, dass Chlorogensäure, die reichlich im Extrakt von grünen Kaffeebohnen vorkommt, das Enzym Glukose-6-Phosphatase hemmt, das die Neubildung von Glukose und die Glukose-Freisetzung durch die Leber auslöst.25,26 Wie bereits erwähnt, ist Glukose-6-Phosphatase eine gefährliche Folge von Zuckerspitzen im Blutzucker.27
Ein anderes Mittel, durch das Chlorogensäure, die Glukosestöße nach der Mahlzeit unterdrückt, besteht in der Hemmung der alpha-Glucosidase. Dieses Darmenzym spaltet komplexe Zucker auf und erhöht deren Absorption im Blut.28 Die Verlangsamung der Resorption üblicher Zucker (einschließlich Saccharose) begrenzt die Glukosespitzen nach der Mahlzeit.29
In einem weiteren wichtigen Mechanismus erhöht Chlorogensäure das Signalprotein für Insulinrezeptoren in Leberzellen.30 Dies führt zu einer Erhöhung der Insulinsensitivität, was wiederum den Blutzuckerspiegel senkt.
 Chlorogenesäure-reiche Pflanzenextrakte senken bei Blutzuckerwerten im Nüchternzustand bei Diabetikern mit schlechtem Ansprechen auf Medikamente mehr als 15 %.31 Eine ähnliche Wirkung wurde bei gesunden Freiwilligen beobachtet, deren intestinale Glukoseaufnahme nach einer Chlorogensäure vermindert war.32
Chlorogenesäure-reiche Pflanzenextrakte senken bei Blutzuckerwerten im Nüchternzustand bei Diabetikern mit schlechtem Ansprechen auf Medikamente mehr als 15 %.31 Eine ähnliche Wirkung wurde bei gesunden Freiwilligen beobachtet, deren intestinale Glukoseaufnahme nach einer Chlorogensäure vermindert war.32
Wurde vor den Mahlzeiten ein Chlorogensäure-Zusatz von 1 Gramm verabreicht, wurden die Glucosespiegel nur 15 Minuten nach oraler Glukose um 13 mg / dl reduziert. Eine Herausforderung, die ihre Fähigkeit demonstriert, die Blutzuckerspitze nach der Mahlzeit beim Menschen schnell zu senken.33
In einer klinischen Studie gaben die Forscher 56 Menschen verschiedene Dosierungen von dem Extrakt aus grünen Kaffeebohnen, standardisiert für Chlorogensäure, an. Fünfunddreißig Minuten später gaben sie den Teilnehmern 100 Gramm Glukose in einem oralen Glukosetest. Der Blutzuckerspiegel sank mit zunehmender Testdosis für Extrakt aus grünen Kaffeebohnen von 200 mg auf 400 mg. Bei der 400-mg-Dosis gab es eine vollständige Abnahme des Blutzuckers um 24% - nur 30 Minuten nach der Glukoseeinnahme.1
Das heißt, wenn Sie einen gefährlichen Glukosewert nach der Mahlzeit von 160 mg / dl hätten, würde der Extrakt aus grünen Kaffeebohnen diesen Wert auf 121 mg / dl reduzieren.
Diese Ergebnisse stehen im Einklang mit den unterstützenden Daten, die die zahlreichen blutzuckersenkenden Wirkmechanismen des grünen Kaffeebohnenextrakts zeigen.
Andere experimentelle Modelle zeigen, dass Chlorogensäure die Genexpression günstig moduliert, um die Aktivität der Leberzellen und den Wert des Hormons Adiponectin zu erhöhen, was die Insulinsensitivität erhöht und entzündungshemmende, antidiabetische und antiatherogene Wirkungen ausübt.34
Vorteile und Einschränkungen des hohen Kaffeeverbrauchs
 Viele epidemiologische Studien deuten auf einen Vorteil des Konsums großer Kaffeemengen hin. Gemäßigte bis hohe Kaffeemengen sind mit einem stark verringerten Risiko für die Entwicklung von Typ-2-Diabetes verbunden.58-61 Laborstudien deuten darauf hin, dass Kaffee Antitumoreffekte gegen Eierstock-, Dickdarm-, Leberkrebs und andere Krebsarten haben kann.62-66 Der Konsum von Kaffee kann mit einem verringerten Schlaganfallrisiko bei Frauen einhergehen, während diejenigen, die gemäßigte Mengen an Kaffee konsumieren, vor akuten Koronarsyndromen geschützt werden können.67,68
Viele epidemiologische Studien deuten auf einen Vorteil des Konsums großer Kaffeemengen hin. Gemäßigte bis hohe Kaffeemengen sind mit einem stark verringerten Risiko für die Entwicklung von Typ-2-Diabetes verbunden.58-61 Laborstudien deuten darauf hin, dass Kaffee Antitumoreffekte gegen Eierstock-, Dickdarm-, Leberkrebs und andere Krebsarten haben kann.62-66 Der Konsum von Kaffee kann mit einem verringerten Schlaganfallrisiko bei Frauen einhergehen, während diejenigen, die gemäßigte Mengen an Kaffee konsumieren, vor akuten Koronarsyndromen geschützt werden können.67,68
Für viele Menschen ist das Trinken großer Mengen Kaffee nicht ideal.
Große Mengen Koffein können reizend sein. In einer Studie wurde festgestellt, dass Personen, die 12 oder mehr Tassen Kaffee täglich tranken, insgesamt 960-1.380 mg Koffein erhielten.69,70 Bei vielen Personen kann ein hoher Koffeinkonsum unerwünscht sein.
Außerdem ist es wichtig anzumerken, dass der kommerzielle Prozess des Röstens von Kaffeebohnen ein Molekül namens HHQ erzeugt, das tatsächlich etwas von der Aktivität der in grünem Kaffee gefundenen Chlorogensäure reduziert.71,72
Ein sehr koffeinarmer Extrakt aus ungerösteten grünen Kaffeebohnen liefert eine standardisierte Dosis nützlicher Chlorogensäure.
Krankheitsrisiken von hochnormalem Blutzucker
 Krebs: Zahlreiche Studien - darunter eine, die in der Online-Ausgabe des Onkologen vom 17 Mai 2010 veröffentlicht wurde, die so groß war, dass sie die Hälfte aller Typ-2-Diabetiker in Schweden einbezog35 - stellten fest, dass die diagnostizierten Diabetiker unabhängig von den bekannten Krebsrisiken, 36-38 ein höheres Risiko der Erkrankung an einigen Krebsarten mit dem Blutzuckerspiegel verbunden war, auch bei Menschen ohne Diabetes. Mit zunehmendem Anstieg der Glukosewerte im Normalbereich stiegen die Risiken für Endometriumkarzinome, 39 Pankreas, 40 Colon, 41,42 und kolorektale Tumore aggressiverer Natur an.43
Krebs: Zahlreiche Studien - darunter eine, die in der Online-Ausgabe des Onkologen vom 17 Mai 2010 veröffentlicht wurde, die so groß war, dass sie die Hälfte aller Typ-2-Diabetiker in Schweden einbezog35 - stellten fest, dass die diagnostizierten Diabetiker unabhängig von den bekannten Krebsrisiken, 36-38 ein höheres Risiko der Erkrankung an einigen Krebsarten mit dem Blutzuckerspiegel verbunden war, auch bei Menschen ohne Diabetes. Mit zunehmendem Anstieg der Glukosewerte im Normalbereich stiegen die Risiken für Endometriumkarzinome, 39 Pankreas, 40 Colon, 41,42 und kolorektale Tumore aggressiverer Natur an.43
Kardiovaskuläre Erkrankungen: Die Probanden wiesen Risiken für kardiovaskuläre Ereignisse, kardiovaskuläre Erkrankungen und kardiovaskuläre Mortalität auf, die in direktem Zusammenhang mit erhöhten, aber immer noch hohen normalen Glukosespiegeln stiegen.44-48 Ein Forscher kommentierte, dass je mehr Blutzuckerspiegel innerhalb der Grenzen, desto geringer ist das kardiovaskuläre Risiko. Das Risiko einer koronaren Herzkrankheit war bei Patienten mit einem Blutzuckerspiegel zwischen 157 und 189 mg / dl nach der Mahlzeit doppelt  so hoch im Vergleich zu einem Risiko unter 144 mg / dL.49Während Diabetes als regelmäßiger Blutzuckerspiegel nach einer Mahlzeit von 200 mg / dl definiert wird, fand ein Forschungsteam ein Schlaganfallrisiko, das anstieg, da der Blutzuckerspiegel im Fasten über 83 mg / dl stieg. Tatsächlich führte jede Erhöhung um 18 mg / dL über 83 zu einem um 27% höheren Risiko, an einem Schlaganfall zu sterben.14
so hoch im Vergleich zu einem Risiko unter 144 mg / dL.49Während Diabetes als regelmäßiger Blutzuckerspiegel nach einer Mahlzeit von 200 mg / dl definiert wird, fand ein Forschungsteam ein Schlaganfallrisiko, das anstieg, da der Blutzuckerspiegel im Fasten über 83 mg / dl stieg. Tatsächlich führte jede Erhöhung um 18 mg / dL über 83 zu einem um 27% höheren Risiko, an einem Schlaganfall zu sterben.14
Kognitive Beeinträchtigung: Mit dem Anstieg des Blutzuckers - entweder im normalen oder im diabetischen Bereich - erhöhte sich das Risiko für diese leichte kognitive Beeinträchtigung und Demenz. 50,51
Nierenerkrankung: Blutzuckerschwankungen begünstigten eine stärkere Produktion von fibrösem Nierengewebe, das zu Nierenerkrankungen führt, als ein hoher, aber konstanter Blutzuckerspiegel.52 Die Autoren der Studie deuteten darauf hin, dass Glukoseschwankungen - mehr als die Mengen selbst - die Ursache der vaskulären Komplikationen bei Nierenschäden sind. In einer anderen Studie wurde ein direkter Anstieg der chronischen Nierenerkrankung festgestellt, da der Hämoglobinwert A1c (ein Marker für die langfristige Glukosekontrolle) anstieg.53
Pankreasfunktionsstörung: Im Pankreas befindliche Betazellen produzieren Insulin, das den Blutzucker steuert. Hohe Blutzuckerwerte können jedoch dazu führen, dass diese Zellen dysfunktional werden und das Risiko für Typ-2-Diabetes steigt. Die Forscher stellten fest, dass eine leichte Betazell-Dysfunktion bereits bei denen nachgewiesen werden konnte, deren Glukosespiegel zwei Stunden nach dem Essen angestiegen war, obwohl sie sich vollständig innerhalb des Bereichs befanden, der von der medizinischen Einrichtung als normal angesehen wurde.54
 Diabetische Retinopathie: Hohe Blutzuckerwerte führen zu diabetischer Retinopathie - Schäden an der Netzhaut, die zu Erblindung führen können. In einer Studie wurde bei 13% der Patienten, die später zu Diabetes überstiegen, und bei 8% der Patienten, die nie zu Diabetes fortgeschritten sind, eine Retinopathie diagnostiziert.55
Diabetische Retinopathie: Hohe Blutzuckerwerte führen zu diabetischer Retinopathie - Schäden an der Netzhaut, die zu Erblindung führen können. In einer Studie wurde bei 13% der Patienten, die später zu Diabetes überstiegen, und bei 8% der Patienten, die nie zu Diabetes fortgeschritten sind, eine Retinopathie diagnostiziert.55
Neuropathie: Wie erwartet zeigten Patienten mit Nervensystemschädigung (Neuropathie), deren Glukosewerte nach der Mahlzeit (nach der Mahlzeit) oberhalb der diabetischen Schwelle lagen, eine Schädigung ihrer großen Nervenfasern. Neuropathie-Patienten, deren Blutzuckerwerte - obwohl erhöht - im normalen Bereich lagen, zeigten jedoch immer noch eine Schädigung ihrer kleinen Nervenfasern. In einem Blutzucker-Bereich, berichtete die Zeitschrift Neurology aus dem Jahr 2003, je höher die Glukose, desto stärker sind die großen Nervenfasern beteiligt.56 Eine weitere Studie mit Nervenschäden im Jahr 2006 bestätigte diese Ergebnisse.57
 Extrakt aus grünen Kaffeebohnen enthält eine natürliche Verbindung (Chlorogensäure), die den Blutzucker durch die Hemmung des Glukose-6-Phosphatase-Enzyms reduziert.
Extrakt aus grünen Kaffeebohnen enthält eine natürliche Verbindung (Chlorogensäure), die den Blutzucker durch die Hemmung des Glukose-6-Phosphatase-Enzyms reduziert.
Glukose-6-Phosphatase erhöht den Blutzucker, indem sie die Bildung von neuer Glukose fördert (Gluconeogenese) und die Freisetzung von in der Leber gespeicherter Glukose induziert (Glycogenolyse).
Diejenigen, deren Glukose im Nüchternzustand über 85 mg / dl liegt oder deren oraler Glukosetoleranztest zweistündige postprandiale Glukosestöße von mehr als 125 mg / dl zeigt, sollten die Einnahme von 200 bis 400 mg standardisierter Extrakte aus grünen Kaffeebohnen in Betracht ziehen. Dies sollte fünf Minuten vor den Mahlzeiten erfolgen.
Um das postprandiale Risiko (nach der Mahlzeit) zu klären, wenn Ihre Nüchternglukose 85 mg / dl beträgt, ein oraler Glukosetoleranztest jedoch nach zwei Stunden einen Blutzuckerwert von über 125 mg / dl aufweist, leiden Sie wahrscheinlich an toxischen Nebenwirkungen. Mahlzeit Glukose-Überspannungen, die durch die Einnahme vom Extrakt aus grünen Kaffeebohnen vor den meisten Mahlzeiten neutralisiert werden können.
Die meisten alternden Menschen leiden sowohl unter Fasten- als auch nach der Prostata-Glukoseüberladung und sollten Schritte einleiten, um das gefährliche Glukose-6-Phosphatase-Enzym zu unterdrücken.
Zusammenfassung
Die Notwendigkeit, Diabetes neu zu definieren, ist kritisch, da das Risiko eines vorzeitigen Todes und einer Erkrankung mit Nüchternblutzucker von mehr als 85 mg / dl stark steigt.
Darüber hinaus bleiben die hinterhältigen Auswirkungen von Blutzuckerspitzen nach einer Mahlzeit weitgehend unentdeckt und setzen die große Mehrheit der Menschen einem erhöhten Krankheitsrisiko aus.
Hinter dieser Gefahr steht die wenig geschätzte Rolle der Glukose-6-Phosphatase bei der Erzeugung und Freisetzung zusätzlicher Glukose ins Blut. Dieses Enzym, das in jungen Jahren zur Regulierung des Blutzuckers beiträgt, kann unangemessen eine gefährliche Nachmahlzeit Überspannung im Blutzucker auslösen, wenn Sie altern.
Avantgarde-Wissenschaftler haben eine bahnbrechende Waffe gefunden, um diese Wogen zu kontrollieren: Extrakt aus grünen Kaffeebohnen. Dieser natürliche Inhaltsstoff enthält eine Verbindung namens Chlorogensäure, die Glukose-6-Phosphatase anspricht und den Blutzuckerspiegel nach dem Verbrauch um bis zu 32% stumpft.
Ein konsistenter Befund bei Personen, die ihre Kalorienzufuhr einschränken, ist ein deutlich niedrigerer Blutzuckerspiegel. Langlebige Enthusiasten können jetzt von einem neuartigen, aber natürlichen Extrakt aus grünen Kaffeebohnen profitieren, um interne Prozesse zu bekämpfen, die gefährliche Blutzuckerwerte verursachen.
Mit Genehmigung von Life Extension verwendetes Material. Alle Rechte vorbehalten.
1. Nagendran MV. Effect of green coffee bean extract (GCE), High in Chlorogenic Acids, on Glucose Metabolism. Poster presentation number: 45-LB-P. Obesity 2011, the 29th Annual Scientific Meeting of the Obesity Society. Orlando, Florida. October 1-5, 2011.
2. Nichols GA, Hillier TA, Brown JB. Normal fasting plasma glucose and risk of type 2 diabetes diagnosis. Am J Med. 2008 Jun;121(6):519-24.
3. Kato M, Noda M, Suga H, Matsumoto M, Kanazawa Y. Fasting plasma glucose and incidence of diabetes—implication for the threshold for impaired fasting glucose: results from the population-based Omiya MA cohort study. J Atheroscler Thromb. 2009;16(6):857-61.
4. Available at: http://diabetes.niddk.nih.gov/dm/pubs/diagnosis/#diagnosis. Accessed August 15, 2011.
5. Glucose tolerance and mortality: comparison of WHO and American Diabetes Association diagnostic criteria. The DECODE study group. European Diabetes Epidemiology Group. Diabetes Epidemiology: Collaborative analysis Of Diagnostic criteria in Europe. Lancet. 1999 Aug 21;354(9179):617-21.
6. Nakagami T. Hyperglycaemia and mortality from all causes and from cardiovascular disease in five populations of Asian origin. Diabetologia. 2004 Mar;47(3):385-94.
7. Miura K, Kitahara Y, Yamagishi S. Combination therapy with nateglinide and vildagliptin improves postprandial metabolic derangements in Zucker fatty rats. Horm Metab Res. 2010 Sep;42(10):731-5.
8. Monnier L, Colette C. Glycemic variability: should we and can we prevent it? Diabetes Care. 2008 Feb;31 Suppl 2:S150-4.
9. Monnier L, Colette C, Owens DR. Glycemic variability: the third component of the dysglycemia in diabetes. Is it important? How to measure it? J Diabetes Sci Technol. 2008 Nov;2(6):1094-100.
10. Triggle CR. The early effects of elevated glucose on endothelial function as a target in the treatment of type 2 diabetes. Timely Top Med Cardiovasc Dis. 2008;12:E3
11. Gerstein HC, Pais P, Pogue J, Yusuf S. Relationship of glucose and insulin levels to the risk of myocardial infarction: a case-control study. J Am Coll Cardiol. 1999 Mar;33(3):612-9.
12. Lin HJ, Lee BC, Ho YL, et al. Postprandial glucose improves the risk prediction of cardiovascular death beyond the metabolic syndrome in the nondiabetic population. Diabetes Care. 2009 Sep;32(9):1721-6.
13. Yu PC, Bosnyak Z, Ceriello A. The importance of glycated haemoglobin (HbA(1c)) and postprandial glucose (PPG) control on cardiovascular outcomes in patients with type 2 diabetes. Diabetes Res Clin Pract. 2010 Jul;89(1):1-9.
14. Batty GD, Kivimäki M, Smith GD, Marmot MG, Shipley MJ. Post-challenge blood glucose concentration and stroke mortality rates in non-diabetic men in London: 38-year follow-up of the original Whitehall prospective cohort study. Diabetologia. 2008 July;51(7):1123-6.
15. Hemmerle H, Burger HJ, Below P, et al. Chlorogenic acid and synthetic chlorogenic acid derivatives: novel inhibitors of hepatic glucose-6-phosphate translocase. J Med Chem. 1997 Jan 17;40(2):137-45.
16. Arion WJ, Canfield WK, Ramos FC, et al. Chlorogenic acid and hydroxynitrobenzaldehyde: new inhibitors of hepatic glucose 6-phosphatase. Arch Biochem Biophys. 1997 Mar 15;339(2):315-22.
17. Rizza RA. Pathogenesis of fasting and postprandial hyperglycemia in type 2 diabetes: implications for therapy. Diabetes. 2010 Nov;59(11):2697-707.
18. Henry-Vitrac C, Ibarra A, Roller M, Merillon JM, Vitrac X. Contribution of chlorogenic acids to the inhibition of human hepatic glucose-6-phosphatase activity in vitro by Svetol, a standardized decaffeinated green coffee extract. J Agric Food Chem. 2010 Apr 14;58(7):4141-4.
19. Salazar-Martinez E, Willett WC, Ascherio A, et al. Coffee consumption and risk for type 2 diabetes mellitus. Ann Intern Med. 2004 Jan 6;140(1):1-8.
20. Pereira MA, Parker ED, Folsom AR. Coffee consumption and risk of type 2 diabetes mellitus: an 11-year prospective study of 28,812 postmenopausal women. Arch Intern Med. 2006 Jun 26;166(12):1311-6.
21. Johnston KL, Clifford MN, Morgan LM. Coffee acutely modifies gastrointestinal hormone secretion and glucose tolerance in humans: glycemic effects of chlorogenic acid and caffeine. Am J Clin Nutr. 2003 Oct;78(4):728-33.
22. Bidel S, Hu G, Sundvall J, Kaprio J, Tuomilehto J. Effects of coffee consumption on glucose tolerance, serum glucose and insulin levels–a cross-sectional analysis. Horm Metab Res. 2006 Jan;38(1):38-43.
23. van Dam RM, Feskens EJM. Coffee consumption and risk of type 2 diabetes mellitus. Lancet. 2002 Nov 9;360(9344):1477-8.
24. Murase T, Misawa K, Minegishi Y, Aoki M, Ominami H, Suzuki Y, Shibuya Y, Hase T. Coffee polyphenols suppress diet-induced body fat accumulation by downregulating SREBP-1c and related molecules in C57BL/6J mice. Am J Physiol Endocrinol Metab. 2011 Jan;300(1):E122-33.
25. Henry-Vitrac C, Ibarra A, Roller M, Merillon JM, Vitrac X. Contribution of chlorogenic acids to the inhibition of human hepatic glucose-6-phosphatase activity in vitro by Svetol, a standardized decaffeinated green coffee extract. J Agric Food Chem. 2010 Apr 14;58(7):4141-4.
26. Andrade-Cetto A, Vazquez RC. Gluconeogenesis inhibition and phytochemical composition of two Cecropia species. J Ethnopharmacol. 2010 Jul 6;130(1):93-7.
27. Bassoli BK, Cassolla P, Borba-Murad GR, et al. Chlorogenic acid reduces the plasma glucose peak in the oral glucose tolerance test: effects on hepatic glucose release and glycaemia. Cell Biochem Funct. 2008 Apr;26(3):320-8.
28. Ishikawa A, Yamashita H, Hiemori M, et al. Characterization of inhibitors of postprandial hyperglycemia from the leaves of Nerium indicum. J Nutr Sci Vitaminol (Tokyo). 2007 Apr;53(2):166-73.
29. Alonso-Castro AJ, Miranda-Torres AC, Gonzalez-Chavez MM, Salazar-Olivo LA. Cecropia obtusifolia Bertol and its active compound, chlorogenic acid, stimulate 2-NBDglucose uptake in both insulin-sensitive and insulin-resistant 3T3 adipocytes. J Ethnopharmacol. 2008 Dec 8;120(3):458-64.
30. Rodriguez de Sotillo DV, Hadley M, Sotillo JE. Insulin receptor exon 11+/- is expressed in Zucker (fa/fa) rats, and chlorogenic acid modifies their plasma insulin and liver protein and DNA. J Nutr Biochem. 2006 Jan;17(1):63-71.
31. Herrera-Arellano A, Aguilar-Santamaria L, Garcia-Hernandez B, Nicasio-Torres P, Tortoriello J. Clinical trial of Cecropia obtusifolia and Marrubium vulgare leaf extracts on blood glucose and serum lipids in type 2 diabetics. Phytomedicine. 2004 Nov;11(7-8):561-6.
32. Thom E. The effect of chlorogenic acid enriched coffee on glucose absorption in healthy volunteers and its effect on body mass when used long-term in overweight and obese people. J Int Med Res. 2007 Nov-Dec;35(6):900-8.
33. van Dijk AE, Olthof MR, Meeuse JC, Seebus E, Heine RJ, van Dam RM. Acute effects of decaffeinated coffee and the major coffee components chlorogenic acid and trigonelline on glucose tolerance. Diabetes Care. 2009 Jun;32(6):1023-5.
34. Zhang LT, Chang CQ, Liu Y, Chen ZM. Effect of chlorogenic acid on disordered glucose and lipid metabolism in db/db mice and its mechanism. Zhongguo Yi Xue Ke Xue Yuan Xue Bao. 2011 Jun;33(3):281-6.
35. Hemminki K, Li X, Sundquist J, Sundquist K. Risk of cancer following hospitalization for type 2 diabetes. The Oncologist. 2010;15(6):548-55. Epub 2010 May 17.
36. Czyzyk A, Szczepanik Z. Diabetes mellitus and cancer. Eur J Intern Med. 2000 Oct;11(5):245-52.
37. Vigneri P, Frasca F, Sciacca L, Pandini G, Vigneri R. Diabetes and cancer. Endocr Relat Cancer. 2009 Dec;16(4):1103-23.
38. Martin-Castillo B, Vazquez-Martin A, Oliveras-Ferraros C, Menendez JA. Metformin and cancer: doses, mechanisms and the dandelion and hormetic phenomena. Cell Cycle. 2010 Mar 21;9(6):1057-64.
39. Cust AE, Kaaks R, Friedenreich C, Bonnet F, et al. Metabolic syndrome, plasma lipid, lipoprotein and glucose levels, and endometrial cancer risk in the European Prospective Investigation into Cancer and Nutrition EPIC. Endocr Relat Cancer. 2007 Sep;14(3):755-67.
40. Rosato V, Tavani A, Bosetti C, et al. Metabolic syndrome and pancreatic cancer risk: a case-control study in Italy and meta-analysis. Metabolism. 2011 May 5.
41. Schoen RE, Tangen CM, Kuller LH, et al. Increased blood glucose and insulin, body size, and incident colorectal cancer. J Natl Cancer Inst. 1999 Jul 7;91(13):1147-54.
42. Aleksandrova K, Boeing H, Jenab M, et al. Metabolic syndrome and risks of colon and rectal cancer: the European Prospective Investigation into Cancer and Nutrition Study. Cancer Prev Res (Phila). 2011 Jun 22.
43. Healy L, Howard J, Ryan A, et al. Metabolic syndrome and leptin are associated with adverse pathological features in male colorectal cancer patients. Colorectal Dis. 2011 Jan 20.
44. Pan WH, Cedres LB, Liu K, et al. Relationships of clinical diabetes and symptomatic hyperglycaemia to risk of coronary heart disease mortality in men and women. Am J Epidemiol. 1986;123:504-16.
45. Wilson PWF, Cupples LA, Kannel WB. Is hyperglycaemia associated with cardiovascular disease? The Framingham Study. Am Heart J. 1991 Feb;121(2 Pt 1):586-90.
46. de Vegt F, Dekker JM, Ruhe HG, et al. Hyperglycaemia is associated with all-cause and cardiovascular mortality in the Hoorn population: the Hoorn study. Diabetologia. 1999 Aug;42(8):926-31.
47. Saydah SH, Miret M, Sung J, Varas C, Gause D, Brancati FL. Post-challenge hyperglycemia and mortality in a national sample of U.S. adults. Diabetes Care. 2001;24:1397-402.
48. Coutinho M, Gerstein H, Poque J, Wang Y, Yusuf S. The relationship between glucose and incident cardiovascular events: a meta regression analysis of published data from 20 studies of 95,783 individuals followed for 12.4 years. Diabetes Care. 1999;22:233–40.
49. Donahue RP, Abbott RD, Reed DM, et al: Postchallenge glucose concentration and coronary heart disease in men of Japanese ancestry. Honolulu Heart Program. Diabetes. 1987 Jun;36 (6):689-92.
50. Tali Cukierman-Yaffe T, Gerstein HC, Williamson JD. Relationship between baseline glycemic control and cognitive function in individuals with type 2 diabetes and other cardiovascular risk factors: the action to control cardiovascular risk in diabetes-memory in diabetes (ACCORD-MIND) trial. Diabetes Care. 2009 Feb;32(2):221-6.
51. Sonnen JA, Larson EB, Brickell K. Different patterns of cerebral injury in dementia with or without diabetes. Arch Neurol. 2009 Mar;66(3):315-322.
52. Polhill TS, Saad S, Poronnik S, Fulcher GR, Pollock CR. Short-term peaks in glucose promote renal fibrogenesis independently of total glucose exposure. Am J Physiol Renal Physiol. 2004 Aug;287(2):F268-73.
53. Bash, LD, Selvin E, Steffes M, Coresh J, Astor BC. Poor glycemic control in diabetes and the risk of incident kidney disease even in the absence of albuminuria and retinopathy: atherosclerosis risk in communities (ARIC) study. Arch Intern Med. 2008 Dec 8/22;168(22):2440-7.
54. Gastaldelli A, Ferrannini E, Miyazaki Y, Matsuda M, De Fronzo RA, San Antonio metabolism study. Beta-cell dysfunction and glucose intolerance: results from the San Antonio metabolism (SAM) study. Diabetologia 2004 Jan;47(1):31-9.
55. Available at: http://docnews.diabetesjournals.org/content/2/8/1.2.full. Accessed August 16, 2011.
56. Sumner CJ, Sheth S, Griffin JW, Cornblath DR, Polydefkis M. The spectrum of neuropathy in diabetes and impaired glucose tolerance. Neurology. 2003 Jan 14;60(1):108-11.
57. Hoffman-Snyder C; Smith BE; Ross MA; Hernandez J; Bosch EP. Value of the oral glucose tolerance test in the evaluation of chronic idiopathic axonal polyneuropathy. Arch Neurol. 2006 Aug;63(8):1075-9.
58. van Dam RM, Feskens EJ. Coffee consumption and risk of type 2 diabetes mellitus. Lancet. 2002 Nov 9;360(9344):1477-8.
59. Rosengren A, Dotevall A, Wilhelmsen L, Thelle D, Johansson S. Coffee and incidence of diabetes in Swedish women: a prospective 18-year follow-up study. J Intern Med. 2004 Jan;255(1):89-95.
60. Huxley R, Lee CM, Barzi F, et al. Coffee, decaffeinated coffee, and tea consumption in relation to incident type 2 diabetes mellitus: a systematic review with meta-analysis. Arch Intern Med. 2009 Dec 14;169(22):2053-63.
61. Salazar-Martinez E, Willett WC, Ascherio A, et al. Coffee consumption and risk for type 2 diabetes mellitus. Ann Intern Med. 2004 Jan 6;140(1):1-8.
62. Butt MS, Sultan MT. Coffee and its consumption: benefits and risks. Crit Rev Food Sci Nutr. 2011 Apr;51(4):363-73.
63. Granado-Serrano AB, Martin MA, Izquierdo-Pulido M, Goya L, Bravo L, Ramos S. Molecular mechanisms of (-)-epicatechin and chlorogenic acid on the regulation of the apoptotic and survival/proliferation pathways in a human hepatoma cell line. J Agric Food Chem. 2007 Mar 7;55(5):2020-7.
64. Kang NJ, Lee KW, Kim BH, et al. Coffee phenolic phytochemicals suppress colon cancer metastasis by targeting MEK and TOPK. Carcinogenesis. 2011 Jun;32(6):921-8.
65. Rakshit S, Mandal L, Pal BC, et al. Involvement of ROS in chlorogenic acid-induced apoptosis of Bcr-Abl+ CML cells. Biochem Pharmacol. 2010 Dec 1;80(11):1662-75.
66. Tai J, Cheung S, Chan E, Hasman D. Antiproliferation effect of commercially brewed coffees on human ovarian cancer cells in vitro. Nutr Cancer. 2010;62(8):1044-57.
67. Larsson SC, Virtamo J, Wolk A. Coffee consumption and risk of stroke in women. Stroke. 2011 Apr;42(4):908-12.
68. Panagiotakos DB, Pitsavos C, Chrysohoou C, Kokkinos P, Toutouzas P, Stefanadis C. The J-shaped effect of coffee consumption on the risk of developing acute coronary syndromes: the CARDIO2000 case-control study. J Nutr. 2003 Oct;133(10):3228-32.
69. Zhang Y, Lee ET, Cowan LD, Fabsitz RR, Howard BV. Coffee consumption and the incidence of type 2 diabetes in men and women with normal glucose tolerance: the Strong Heart Study. Nutr Metab Cardiovasc Dis. 2011 Jun;21(6):418-23.
70. Available at: http://www.ico.org/caffeine.asp. Accessed July 21, 2011.
71. Suzuki A, Fujii A, Yamamoto N, et al. Improvement of hypertension and vascular dysfunction by hydroxyhydroquinone-free coffee in a genetic model of hypertension. FEBS Lett. 2006 Apr 17;580(9):2317-22.
72. Yamaguchi T, Chikama A, Mori K, et al. Hydroxyhydroquinone-free coffee: a double-blind, randomized controlled dose-response study of blood pressure. Nutr Metab Cardiovasc Dis. 2008 Jul;18(6):408-14.


